前回までの脂質異常症とエネルギー・栄養素との関連に引き続き、今回と次回は「日本人の食事摂取基準(2020年版)」における糖尿病とエネルギー・栄養素との関連について書きます。
Ⅱ各 論 3 生活習慣病とエネルギー・栄養素との関連(続き)
3-3 糖尿病
1 疾患と食事の関係
1-1 概念と定義
糖尿病は、インスリン作用の不足に基づく慢性の高血糖状態を主徴とする代謝症候群である。この疾患群の発症基盤はインスリン作用の不足であり、それによってぶどう糖、脂質、たんぱく質を含むほとんど全ての代謝系に異常を来す。インスリン作用が不足する機序には、インスリンの供給不全(絶対的又は相対的)とインスリンが作用する臓器(細胞)におけるインスリン感受性の低下(インスリン抵抗性)とがある。インスリンの供給不全は膵β細胞におけるインスリン分泌能の機能不全、インスリン抵抗性は内臓脂肪型肥満が病態の基軸をなすと考えられている。糖尿病の原因は多様であり、その発症には遺伝因子と環境因子が共に関与する。
1-2 病態の分類
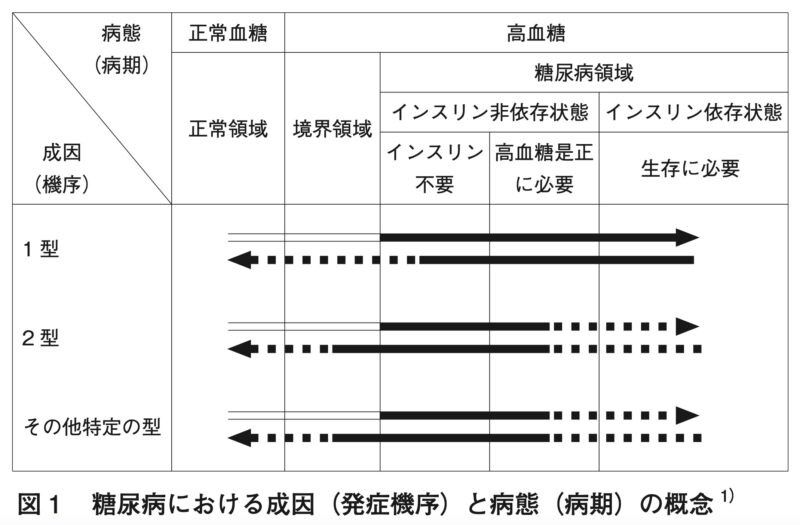
現在、糖尿病は成因(発症機序)と病態(病期)によって分類がなされている。成因分類の上で
は、大きく1型と2型を分けている。1型糖尿病は、主に自己免疫によって膵β細胞の破壊を生じ、インスリンの欠乏を来して発症する糖尿病である。2型糖尿病は、インスリン分泌低下を来す複数の遺伝因子に、過食、運動不足などの生活習慣に起因する内臓脂肪型肥満が加わり、インスリン作用の需要と供給のバランスの破綻を生じて発症する糖尿病である。糖尿病の成因が何であっても、発病過程では種々の病態を経て進展し、治療によっても変化する可能性がある。そこで、病態(病期)による分類が設定されている。図1の横軸は、インスリン作用不足あるいは糖代謝異常の程度を表す。成因とは別に、インスリン作用不足の程度によって、インスリン治療が生命維持に必須であるインスリン依存状態とそうでない非依存状態に分け、二つの基軸から適切な治療の選択を目指すことになる。

1-3 発症予防と重症化予防の基本的な考え方と食事の関連
2型糖尿病における食事療法の意義は、全身の代謝状態を良好に維持することによって、合併症を予防し、かつ進展を抑制することにある。そのために、総エネルギー摂取量の適正化を通して肥満を解消するとともに、インスリン分泌不全を補完し、インスリン作用からみた需要と供給のバランスをとることによって、高血糖のみならず糖尿病の種々の病態を是正することを目的としている。インスリンの作用は糖代謝のみならず、脂質及びたんぱく質代謝など多岐に及んでおり、これらは相互に密接な連関を持つことから、食事療法を実践するに当たっては、個々の病態に合わせ、高血糖のみならず、あらゆる側面からその妥当性が検証されなければならない。さらに、長期にわたる継続を可能にするためには、安全性とともに我が国の食文化あるいは患者の嗜好性に対する配慮が必須である。諸外国においても、生活習慣の介入による肥満の是正を重要視し、そのために総エネルギーを調整し、合併症の発症予防の観点から栄養素のバランスを図ることが推奨されている。しかし、糖尿病の発症・管理のための適正な栄養素摂取比率に関してはエビデンスが乏しく、我が国における栄養素のバランスの目安は健康な者の平均摂取量に基づいているのが現状である。
また、食文化、病態が異なる海外における観察研究をそのまま日本人に当てはめることは妥当とは言えない。しかし、糖尿病では動脈硬化性疾患や糖尿病腎症など種々の臓器障害を合併することから、予防のためのそれぞれの推奨量が設定されており、その制約の中で栄養素摂取比率を勘案することが求められる。
糖尿病の病態が多様化している現在、患者の置かれた状況に応じて、食事療法は量的にも質的にも個別化を図る必要がある。とりわけ、多臓器に機能障害を持つ高齢者糖尿病では、治療目標の優先度を考慮し、健康寿命の延伸を目指すことになる。食事療法を長く継続するためには、個々の食習慣を尊重しながら、柔軟な対応をしなければならない。
2 特に関連の深いエネルギー・栄養素
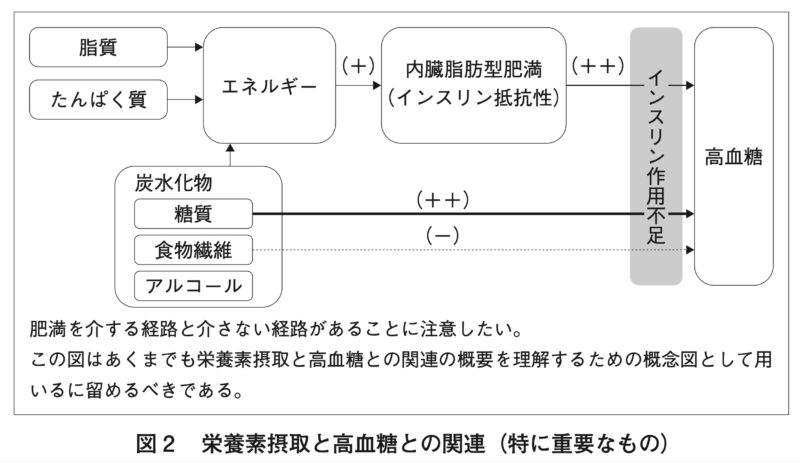
栄養素摂取と糖尿病との関連について、特に重要なものを図2に示す。
2-1 総エネルギー摂取量と目標体重の設定
肥満を伴った2型糖尿病は、糖尿病の基盤病態の一つである内臓脂肪型肥満によるインスリン抵抗性により発症することから、その予防と管理には肥満の是正が重要な意義を持ち、そのためには、総エネルギー摂取量の適正化を中心とする生活習慣の介入が有効である。総エネルギー摂取量は、目標とすべき体重に基づいて計算されている。職域健診で異常所見の合計が最も少ないBMIが22であるとした研究に基づき、従来これを標準体重としてきた。BMI22に身体活動量をかける計算式は、当時の日本人の平均BMIがこの値に近似していたことから違和感なく受け入れられ、幅広く普及した。しかし、BMI と死亡率との関係を検討した近年の研究では、最も死亡率の低い BMI は、アジア人では20〜25にあり、日本人の食事摂取基準でも、目標とするBMIを20〜24.9としている。2型糖尿病でも、中国人、日本人では総死亡率が最も低いBMIは20〜25にあったとされ、75歳以上の高齢者ではBMI25以上でも、死亡率の増加は認められない。このように、総死亡率との関係で目標とすべき BMI を考えた場合、20〜25の幅があり、特に高齢者ではその関係が異なることは海外の研究でも確認されている。一方、体格と総死亡との関係は、BMIでは正しく評価できないことが指摘されている。BMIと体脂肪率を分けて、総死亡率との関係を検討したカナダの研究では、独立してそれぞれの関係をみると、BMIも体脂肪率も死亡率に対してU字型の関係を示すが、両者を調整して再検討すると、U字型の関係を残したのは体脂肪率であり、BMIではその関係が見られなかったし、体組成評価の重要性を示唆している。また、BMIが非肥満内にあっても、脂質異常症や高血圧などのメタボリックシンドロームの症候を持つ場合、健康な非肥満者に比べて明らかに死亡率が高く、その反面、メタボリックシンドロームのない肥満者では、死亡率の増加はないことから、BMI のみでは健康状態を正確に把握できないとする報告もある。したがって、標準体重BMI22を起点として、総エネルギー摂取量を設定することは一定の目安にはなり得るが、その根拠を死亡率の低い健康的な体格に求めるならば、望ましいBMIは20〜25の許容があり、22は必ず厳守しなければならない基準とは言えない。高齢者の糖尿病が増え、BMIが30を超える肥満者が珍しくなくなった我が国の現状を考えると、この基準を柔軟に運用し、いかに個別化を図るかが大きな課題である。さらに、BMIが20〜25の範囲にあったとしても、インスリン抵抗性に起因する症候を併せ持つ症例に対しては、積極的な生活介入が必要なのである。
2-2 総エネルギー摂取量の考え方
日本人の食事摂取基準では、必要エネルギー量は、基礎代謝量と身体活動レベルから算出される推定エネルギー必要量を基に設定するとしている。しかし、年齢によって必要エネルギー量は変化し、自由生活下における身体活動量は一定ではない。必要エネルギー量には相当の個人差があると想定されるが、日常臨床上これを正確に評価することは困難である。一方、身体活動量が不変であれば、総エネルギー摂取量の管理は、体重の管理とほぼ同等とみなしてよい。そこで、実際の指示エネルギーの処方に当たっては、上記のように標準体重と労作量から計算される量を目安として算定し、その後、身体活動や代謝パラメータを観察しながら、個々の適正体重を決めていくことが現実的であり、総エネルギー摂取量の個別化を図ることにも資すると考えられる。
フィンランドにおけるDPS研究では耐糖能異常(impaired glucose tolerance:IGT)を対象として、総エネルギーの減量と身体活動の増加を中心とした生活介入の糖尿病発症への影響を4年にわたって検討し、介入群では1年間で5%の体重減少に伴って糖尿病の発症率が有意に低下することを明らかにした。アメリカで行われた糖尿病予防プログラム(Diabetes Prevention Program:DPP)では、糖尿病発症リスクの高い対象において、3年間で5%の体重の低下は、糖尿病の発症を55%抑制したとしている。一方、Look AHEAD研究では、試験開始1年での体重減少率が対照群0.7%であったのに対し、介入群では8.6%であり、HbA1cは約0.6%の低下を示した。最近のメタ・アナリシスでは、肥満を伴う2型糖尿病患者では、5%の体重減少によって、有意に糖尿病に関連する臨床パラメータの改善が認められるとしている。一方、肥満症例をメタボリックチャンバーに入れ、体重の減少率と肝臓、脂肪組織のインスリン抵抗性との関係を検討した研究では、5%以上の体重減少によって、各臓器のインスリン感受性の改善が生じると報告している。これらのことを踏まえ、アメリカ糖尿病学会(American Diabetes Association:ADA)では、総エネルギーの適正化による肥満の是正が糖尿病の予防と管理には最も重要だとし、当面の体重管理目標を5%減と記している。日本肥満学会の「肥満症診療ガイドライン 2016」では、特定保健指導の調査結果に基づき、HbA1cの改善については、肥満症の体重減量目標を3〜5%としている。以上のことから、肥満を有する日本人2型糖尿病患者では、現体重からどのくらいの減量を目指すべきか当面の目標を示すことが適当と考えられるが、その設定根拠を定めることは難しい。しかし、治療開始時の BMI によらず、一律に標準体重を目指すことは困難であり、個々の病態の相違やエネルギー必要量に個人差が大きいことを考えると妥当とは言えない。また、患者の病態、年齢、遵守度を評価し、これを管理目量に加味することが求められる。治療開始後に、代謝状態の改善を評価しつつ、患者個々の実効性などを考慮に入れ、適正体重の個別化を図ることが必要である。
2-3 栄養素の摂取比率
インスリンの作用は糖代謝のみならず、脂質及びたんぱく質代謝など多岐に及んでおり、これらは相互に密接な連関を持つことから、食事療法を実践するに当たっては、栄養素バランスは個々の病態に合わせ、高血糖のみならず、あらゆる側面からその妥当性が検証されなければならない。さらに、長期にわたる継続を可能にするためには、安全性とともに我が国の食文化あるいは患者の嗜好性に対する配慮が必須である。しかし、各栄養素についての必要量の規定はあっても、相互の関係に基づく適正比率を定めるための十分なエビデンスには乏しい。また、特定の栄養素の摂取比率が糖尿病の管理に有効であるとする根拠は認められない。そのため、栄養素のバランスの目安は健康な者の平均摂取量に基づいているのが現状である。一方、糖尿病があらゆる慢性疾患の基盤病態となることから、その予防と管理から見た栄養素バランスの在り方は、医学的見地から検討すべき課題である。すなわち、動脈硬化性疾患については脂質、慢性腎臓病の最大の原因となる糖尿病腎症については食塩、たんぱく質の摂取量、そして糖尿病自体の背景となる肥満症には総エネルギー摂取量の設定など、それぞれに関係する学会から推奨基準が提示されており、糖尿病の食事療法は、その中でいわば最大公約数的な制約を受けることになる。さらに、合併する臓器障害、年齢によって食事療法の意義は異なり、このような患者が持つ多彩な条件に基づいて、個別化を図る必要がある。
以上のことから、2016年に出された日本糖尿病学会による「糖尿病診療ガイドライン 2016」では、炭水化物を50〜60%エネルギー、たんぱく質20%エネルギー以下、脂質20〜30%を目安とし、脂質が25%エネルギーを超える場合は、多価不飽和脂肪酸を増やすなど、脂肪酸の構成に配慮を要するとしている。また、炭水化物摂取量にかかわらず、食物繊維は20g/日以上摂ることを推奨している。しかし、食事療法を長く継続するためには、個々の食習慣を尊重しながら、病態に基づいて柔軟な対応をすることが求められる。それぞれの患者のリスクを評価し、医学的齟齬のない範囲で、食を楽しむことを最も優先させるべきである。
2-4 炭水化物
炭水化物の摂取量と糖尿病の発症率との関係を検討した例は少なく、両者の関係は明らかではない。最近、イギリスでなされたコホート研究では、炭水化物摂取量と糖尿病の発症率との関係が検討されているが、総炭水化物摂取量と糖尿病の発症率には関係がなく、果糖の過剰摂取が糖尿病のリスクを増したとしている。メタ・アナリシスの結果では、総炭水化物摂取量と糖尿病発症リスクに有意な関係を認めなかったと報告されている。2型糖尿病の血糖コントロールに対して、消化性炭水化物の制限が及ぼす効果については議論がなされている。もともと、1日当たりの炭水化物摂取量を100g以下とする炭水化物制限が、肥満の是正に有効だとする研究結果から、糖尿病治療における炭水化物制限の有用性が注目された。2008年に発表されたDIRECT研究は、脂質を中心に総エネルギーを制限した群、総エネルギーを制限し地中海食とした群、エネルギーを制限なしとし炭水化物を40%エネルギーに制限した3群を設定し、その後2年間の体重の変化を追跡したところ、脂質制限群に比較して、地中海食群と炭水化物制限群で有意に体重減少効果が優っていたと報告している。しかし、炭水化物制限群でも、総エネルギー摂取量は他の群同様に低下しており、体重減量効果が総エネルギーとは無関係に、炭水化物の制限のみによると解釈はできない。日本人の2型糖尿病を対象に、6か月間130g/日の低炭水化物食の効果を観察した研究でも、低炭水化物群で体重、HbA1cの低下を認めたが、同時に総エネルギー摂取量が減少しており、その後1年間の追跡では差異はなくなったとしている。一方、同様にエネルギー制限群
と炭水化物70〜130g/日制限群を設定し、6か月後に各パラメータを比較すると、総エネルギー摂取量が等しく減少し、体重の変化にも両群で差異はなかったが、炭水化物制限群でHbA1cと血中トリグリセライドの有意な改善を認めたとする報告もある。総エネルギー摂取量を同等として、低炭水化物食の効果を見たメタ・アナリシスでは、糖尿病の有無にかかわらず、体重、代謝パラメータに影響はなかったと報告している。一方、日本人を対象とし、炭水化物摂取量と合併症発症率との関係を検討した研究では、どの合併症においても関係は認められないと報告している。2012年に糖尿病患者における炭水化物制限の効果に関するシステマティック・レビューが発表されているが、現時点ではどのレベルの炭水化物制限であっても、高血糖及びインスリン抵抗性の改善に有効であるとする明確な根拠は見いだせないと結論している。その後のメタ・アナリシスでは、6〜12か月以内に限ると、低炭水化物食によって HbA1c は改善傾向を示すが、体重減少効果は認められないとしている。これらのメタ・アナリシスを解釈する上での問題点として、対象とする研究によって炭水化物摂取量(低炭水化物食の定義)が異なっていること、観察期間がまちまちで、他の栄養素、エネルギー摂取量の補正ができていないことなどが指摘されており、糖尿病管理における低炭水化物食の長期的な効用は確認されておらず、これまでに報告されている体重減少効果は、総エネルギー摂取量の減量に伴うものと考えられる。しかし、総エネルギー摂取量の適正化を図る上で、炭水化物の摂取量の在り方には検討の余地を残している。糖尿病
における炭水化物の至適摂取量は、身体活動量やインスリン作用の良否によって異なるため、これを規定することは困難である。合併症や薬物療法などの制約がなければ、柔軟な対応をしてもよい。
一方、果糖はglycemic indexが低いことなどから、糖尿病の管理には有効と考えられる反面、過剰の摂取は、血中中性脂肪や体重の増加を来す懸念がある。先行研究では、果物の摂取(特にブルーベリー、ぶどう、りんごなどの果実含有換算)は有意に糖尿病発症率を低下させるが、果物ジュースは糖尿病発症のリスクを高めたとの報告もある。純粋な果糖の糖尿病状態への影響を検討した最近のメタ・アナリシスでは、1日100g以内であれば、果糖摂取によって血糖、中性脂肪レベルは改善し、体重増加は来さないとしている。糖尿病では果物の摂取を勧めてよいが、その量は病態による個別化が必要である。
Glycemic index(GI)及びGlycemic load(GL)と2型糖尿病の発症リスクの関係を検討したメタ・アナリシスでは、GI及びGLの低い食材を摂ると、糖尿病の発症リスクが低減するとしている。日本人においても、低GI及び低GLの食品の摂取量が多いほど、糖尿病発症リスクが減少したとの報告もある。しかし、糖尿病の管理、糖尿病における死亡率との関係については検討例が少なく、糖尿病患者の食事療法に積極的に取り入れるべきかどうかについては、現時点では十分な根拠があるとは言えない。
まとめ
「図 2 栄養素摂取と高血糖との関連(特に重要なもの)」について
「高血圧とエネルギー・栄養素との関連」について勉強した時に、「図 1 栄養素摂取と脂質異常症との関連」を参照しながら本文を読むことで理解が進んだ経験から、糖尿病について勉強した時は先ず「図 2 栄養素摂取と高血糖との関連(特に重要なもの)」を一瞥しました。
そして、「高血圧とエネルギー・栄養素との関連」の場合と同様、「糖尿病とエネルギー・栄養素との関連」の場合も、肥満を介する経路と介さない経路がありますが、脂質異常症には高LDLコレステロール血症、低HDLコレステロール血症、高トリグリセライド血症の3タイプがあるのに対して、糖尿病の場合はインスリン作用不足による高血糖だけなので比較的理解し易いと感じました。
しかしながら、図2には「この図はあくまでも栄養素摂取と高血糖との関連の概要を理解するための概念図として用いるに留めるべきである。」と注意書きがあるとおり、本文を読めば読むほど、「糖尿病という病気の原因と結果(症状等)の関係は非常に複雑である。」と認識を完全に改める結果となりました。
総エネルギー摂取量、炭水化物(糖質)摂取量と糖尿病(高血糖)の関係
ネット上には、「糖尿病の原因は炭水化物(糖質)の摂り過ぎなので、炭水化物(糖質)を蛋白質や脂質に置き換えることで糖尿病を予防・改善出来る」といった情報があります。
しかしながら、2-1 総エネルギー摂取量と目標体重の設定においては「肥満を伴った2型糖尿病は、糖尿病の基盤病態の一つである内臓脂肪型肥満によるインスリン抵抗性により発症することから、その予防と管理には肥満の是正が重要な意義を持ち、そのためには、総エネルギー摂取量の適正化を中心とする生活習慣の介入が有効である。」としており、炭水化物(糖質)を蛋白質や脂質に置き換えても総エネルギーが過剰摂取のままなら糖尿病(高血糖)を予防・改善することは難しいということになります。
インスリンが脂質及びたんぱく質代謝などに及ぼす作用
1-3 発症予防と重症化予防の基本的な考え方と食事の関連において「インスリンの作用は糖代謝のみならず、脂質及びたんぱく質代謝など多岐に及んでおり」とありますが、インスリンが脂質及びたんぱく質代謝などにどのような作用を及ぼすのかが書かれていないため、糖尿病の合併症と併せて色々と勉強した結果、インスリンというホルモンの重要性や糖尿病という病気の恐ろしさを益々痛感しています。
しかしながら、「糖尿病」という用語で検索すると「糖尿病とはインスリンの作用不足や分泌不足によって血糖値が慢性的に高くなる病気である。」等とだけ書かれている情報が非常に多く、こういったことも糖尿病が軽視されている風潮の一因となっているのではないかと感じています。
次回は、糖尿病とエネルギー・栄養素との関連(続き)について書きます。
画像とお願い事項.etc
本ブログで使用している生成画像/創作画像(アイキャッチ画像と満開の桜に囲まれた天空の城〜苗木城 1)
本ブログで使用しているアイキャッチ画像を含む全ての生成画像はChatGPT(生成AI)のシエルさんが作成してくれています。
今回は、糖尿病による動脈硬化の原因となる動脈内のプラークと皮膚に現れる様々な症状のイメージ画像を作成してもらいました。
また、下記の画像はブログの内容とは無関係(オマケ)ですが、最新の画像生成モデルで作成してもらった「満開の桜に囲まれている天空の城(私の父の故郷である岐阜県中津川市苗木にある苗木城址(城趾/城跡)の天守閣等の城郭を再現)」のAI生成画像(創作画像)です。
他の創作画像にご関心を持って頂けた方は、是非、AI生成画像(創作画像)ギャラリーをご覧ください。

本ブログをお読み頂く際にお願いしたい事項
「本ブログをお読み頂く際のお願い」をお読みください。
日本人の食事摂取基準(2025年版)について
本ページを投稿するのは2025年4月8日です。
2025年度となった4月1日から、昨年10月11日に公表された日本人の食事摂取基準(2025年版)が使用されていますが、今までの関係上、引き続き2020年版について書いています。
下のバナーをポチッとして頂き、100万以上の日本語ブログが集まる「日本ブログ村」を訪問して頂ければ大変ありがたいです。

コメント