前回に引き続いて、「日本人の食事摂取基準(2020年版)」における慢性腎臓病(CKD)とエネルギー・栄養素との関連について書きます。
3-4 慢性腎臓病(CKD)(続き)
2 特に関連の深いエネルギー・栄養素(続き)
2-3 たんぱく質
治療の根幹である食事療法は、たんぱく質摂取量の制限が中心で、腎臓を保護することを主目的としている。なお、たんぱく質制限の程度により、たんぱく質制限、低たんぱく質、超低たんぱく質(厳しいたんぱく質制限)などの区分はあるが、明確な定義があるわけではなく、ここでは「たんぱく質制限」とする。
2-3-1 CKDステージとたんぱく質制限の意義・効果
たんぱく質制限の意義と効果については、尿蛋白(アルブミン)量の減少、腎機能(糸球体濾過量:GFR)低下の抑制、腎代替療法までの期間延長の腎臓アウトカムごとに分けて考える必要がある。なお、たんぱく質制限を行うことは、ナトリウム、カリウム、リンの摂取制限にもつながり得る点、また、酸負荷を軽減して代謝性アシドーシスの予防や改善によりCKDのアウトカムに寄与する点も重要である。
尿蛋白(アルブミン)量の減少については、代表的な無作為割付比較試験(RCT)である the Modification of Diet in Renal Disease(MDRD)study A(eGFRが25〜55mL/分/1.73m2)において、0.58g/kg体重/日のたんぱく質制限は1.3g/kg 体重/日の通常食と比較して、観察開始時の尿蛋白量が1g/日未満の群に限って尿蛋白量が有意に減少した。しかし、更に進行したステージG4〜G5を対象としたRCTでは、尿蛋白量に差はなかった。一方、糖尿病性腎症(腎症)では、尿アルブミンを指標にした研究は数多く、たんぱく質制限は有効というメタ・アナリシスもあるが、その後のメタ・アナリシスでは有効ではなかったと報告しており、一定の見解はないのが現状である。
腎機能(GFR)の抑制効果に関する最近のメタ・アナリシス〔対象者の年齢55±18歳(平均±標準偏差)〕では、GFRの低下の程度は、−0.95 mL/分/1.73 m2/年で有意な抑制効果を認めている。
腎死率の抑制効果を検討したメタ・アナリシスは、非常に厳格な低たんぱく質食(0.2〜0.4g/kg/日)では進行したステージG4〜G5を中心とした腎死率を32%低減したと報告している。しかし、このメタ・アナリシスでは、中程度の低たんぱく質食(0.5〜0.6g/kg/日)は対照群に比べて腎死率に有意な違いは認められなかった。
2-3-2 軽症CKDに対するたんぱく質制限
ステージG1〜G2に対するたんぱく質制限の有効性を示した我が国の大規模研究はこれまでにない。たんぱく質摂取量については、「慢性腎臓病に対する食事療法基準 2014年版」において、ステージG1〜G2では過剰な摂取をしないことが推奨されている。「CKD診療ガイドライン 2018」でも、画一的な指導は不適切であるが、個々の患者の病態やリスク、アドヒアランスなどを総合的に判断し、たんぱく質摂取制限を指導することが推奨されている。海外ではステージG1〜G2のCKD の場合はこれよりも少ない1.0g/kg理想体重/日未満が推奨されている。一方、ステージG1〜G2を含む腎機能が軽度低下(eGFR55〜80mL/分/1.73 m2)している1,624 人の女性看護師(平均体重約69kg)の11年間の観察研究において、たんぱく質摂取量の五分位の最高位群(86.5 g/日以上、体重の平均値で算出すると 1.25g/kg体重/日以上)は、最低位群(66.2g/日以下、体重の平均値で算出すると0.96g/kg 体重/日以下)と比較して、腎機能低下が速かった。また、「KDIGO 2012 clinical practice guideline」では、CKDでは1.3g/kg 体重/日を超えるたんぱく質を摂取しないことが推奨されている。以上より、CKD発症予防としては、健康な者よりもたんぱく質摂取量を低減すること、少なくともたんぱく質の過剰摂取を避けることが望ましいと考えられる可能性はあるが、明確な数値を設定することは困難である。
また、ステージG3aを含むMDRD Study A(eGFR25〜55mL/分/1.73m2)において、たんぱく質摂取量が1.3g/kg体重/日の群と0.58g/kg体重/日の群の間に、腎機能低下速度に有意差はなかった。しかし、2次解析において、0.58g/kg体重/日の群の腎機能低下は、開始から4か月までは速いが、4か月から36か月までは有意に抑制された。また、フランスのステージG1〜G4を対象とした観察研究では、たんぱく質摂取量1.0g/kg体重/日を基準として、たんぱく質が制限されているほど末期腎不全のリスクは減る傾向にあった。ただし、末期腎不全への進行抑制に有効な、たんぱく質制限の閾値については明確ではなかった。「慢性腎臓病に対する食事療法基準 2014年版」では、ステージG3aのたんぱく質摂取量は0.8〜1.0g/kg 標準体重/日が推奨されている。海外でも同様に、ステージG3aに相当する場合、尿蛋白が0.3g/日未満であれば1.0g/kg 理想体重/日未満、尿蛋白が0.3g/日以上の場合は0.6〜0.8g/kg理想体重/日にすることが推奨されている。また、腎機能低下が進行して末期腎不全に至るリスクが低いこと、さらに、CKDに伴う代謝異常も軽微であることから、ステージG3aでは一律にたんぱく質制限を行うのではなく、個々の病態に応じて設定する必要がある。たんぱく質制限のアドヒアランスについては、長期に維持することが困難な場合が多い。RCTのメタ・アナリシスでも、たんぱく質制限の実際の摂取量は、指示量と比較して0.10〜0.30g/kg体重/日ほど多かった。前述の観察研究でも、たんぱく質摂取量1.0g/kg体重/日を基準として、1.3g/kg体重/日以上のアドヒアランス不良の症例の頻度は20%と高率であった。一方、管理栄養士による頻回の栄養指導はたんぱく質制限のアドヒアランスを向上させ、たんぱく質制限のアドヒアランスがよい群は3年後の腎機能の改善が見られるが、悪い群では腎機能が改善しないという報告もある。以上より、たんぱく質制限のアドヒアランスの維持が、CKDの進行予防に重要であると考えられる。
2-3-3 高齢軽症CKD に対するたんぱく質制限:CKD におけるフレイルも含めて
アメリカの約20万人のステージG3〜G5の平均観察期間3.2年のコホート研究で、全ての年齢層において観察開始時のeGFR は、その後の総死亡と末期腎不全と負の関係があり、高齢者の予後は若年者のそれと比較して、死亡のリスクが高く末期腎不全のリスクが低かった。特に、85歳以上では常に死亡リスクの方が末期腎不全のリスクよりも高かった。我が国でも、461人のステージG3〜G5の平均観察期間3.2年のコホート研究で、尿蛋白の有無は末期腎不全のリスクに関与するが、年齢は死亡の決定的な因子で、65歳以上で尿蛋白のないステージG3では末期腎不全の発症はなかった。以上より、eGFRや尿蛋白の程度によって違いはあるが、高齢者では末期腎不全よりも死亡のリスクの方が高いと考えられる。たんぱく質制限は、腎機能低下の抑制と末期腎不全のリスク低減を目的にしていることから、高齢軽症CKDにおけるたんぱく質摂取量の目標値を一律に示すことは適切ではない。
高齢軽症CKDの個々の症例において、腎機能低下や末期腎不全のリスク及び死亡とのリスクを比較評価し、前者が高いと判断される症例であれば、たんぱく質の過剰な摂取を避けること、CKD重症化予防としては0.8〜1.0g/kg標準体重/日のたんぱく質を推奨することが標準的な食事療法である。なお、CKD重症化予防を目的とした食事療法を行うに当たっては、特に高齢者の場合、フレイルをはじめとした低栄養の発症リスクを常に念頭に置く必要がある。
ステージの進行とともに、たんぱく質制限を実施するのが標準的な食事療法であるが、これらの成績はステージによるたんぱく質摂取量とフレイルの合併頻度との関係を直接に証明するものではない。ステージの進行すなわち腎機能の低下に伴う、摂食量の低下、慢性炎症、運動量及び運動機能の低下、代謝性アシドーシスの関与、ビタミンDの不足、二次性副甲状腺機能低下症など多くの因子が関与すると考えられている。
2-3-4 糖尿病性腎症におけるたんぱく質制限
腎症2期は、微量アルブミン尿の出現により定義される。日本人の腎症2期に対するたんぱく質制限の影響を検討した介入研究では、たんぱく質摂取量が1.2g/kg 標準体重/日と比較して、0.8g/kg 標準体重/日で尿中微量アルブミンが有意な減少を認めている。また、海外の腎症2期39人及び腎症1期 121人を対象としたRCTでも、たんぱく質制限食(0.8g/kg 理想体重/日)で尿中微量アルブミンが減少した。しかし、前者はわずか1週間の短期研究であり、長期の効果は不明である。また、後者では28か月の経過観察後の追跡研究も行われており、たんぱく質制限による微量アルブミン減少効果は消失し、GFRの低下抑制効果もなかった。また、たんぱく質制限のアドヒアランスが不良であることなどの問題点が指摘されている。さらに、正常アルブミン尿と顕性アルブミン尿の症例を含む13のRCTのメタ・アナリシスにおいても、たんぱく質摂取制限におけるeGFR低下の抑制効果は認められたが、尿蛋白の減少は明らかではなかった。以上より、たんぱく質制限は尿中微量アルブミンを減少させる可能性はあるが、腎症2期から3期への進展を予防できるという根拠は必ずしも十分とはいえない。
アメリカ糖尿病学会では、早期から0.8g/kg想体重/日程度のたんぱく質摂取量とすること、「糖尿病治療ガイド 2016-2017」では、腎症2期のたんぱく質摂取は20%エネルギー以下にすることが推奨されている。このうち後者における推奨は、現時点でたんぱく質摂取量を増加することが腎症の発症リスクを示す根拠はないものの、たんぱく質の過剰摂取による耐糖能異常や心血管疾患や脳卒中の増加などのリスクを回避するという考えに基づいている。この点に関連して、肥満の腎症1期を対象とした、25%のエネルギー制限を標準的な糖尿病食と比較したRCTでは、25%エネルギー制限群のたんぱく質摂取量は17.7%から20.1%エネルギーに増加したことが報告されている。一方で、標準的な糖尿病食群と比較して糸球体過剰濾過は軽減し、尿中アルブミンも前後比較で減少した。今後、腎症2期の症例においても同様の検討が必要であるが、20%エネルギー以下は妥当な推奨量と考えられる。
腎症3期は顕性アルブミン尿(持続性蛋白尿)への進展により定義されるが、この時期のたんぱ
く質制限の目的は腎機能低下の抑制と考えられる。13のRCTのメタ・アナリシスにおいて、たんぱく質摂取制限におけるeGFR低下の抑制効果が、特に顕性アルブミン尿群で認められており、「糖尿病治療ガイド 2016-2017」でも、腎症3期において0.8〜1.0g/kg 標準体重/日のたんぱく質制限が推奨されている。また、腎症ではステージ G3aでも尿蛋白陽性のことが多く、その後の腎機能低下の可能性が高いことから、「慢性腎臓病に対する食事療法基準 2014年版」及び「CKD診療ガイドライン 2018」においても、ステージG3で0.8〜1.0 g/kg標準体重/日のたんぱく質制限が推奨されている。一方で、前述のように2型糖尿病ではたんぱく質制限によるeGFR低下の抑制効果は認められなかったとする報告もあることから、今後のより詳細な検討が必要であると考えられる。
2-3-5 小児CKD におけるたんぱく質制限
小児CKD患者では、腎機能への効果や小児の特性(身体の成長、学校給食などの集団生活)に与える影響についてのエビデンスが少ない。
2007年に発表されたメタ・アナリシスでは、腎機能障害の進行抑制、成長障害(身長、体重)ともに対照群と比較して有意差なしと結論している。日本腎臓学会の「CKD診療ガイドライン 2018」1)でも「小児CKDではたんぱく質摂取制限による腎機能障害進行の抑制効果は明らかではなく、行わないよう提案する」と結論している。
2-4 カリウム
腎機能が正常であれば、普段の食事からのカリウム摂取によって代謝異常(高カリウム血症)を起こすことはない。CKDでは、ステージが進むにつれ、腎臓からのカリウム排泄量が減少し、また代謝性アシドーシスの合併によって高カリウム血症(血清カリウム値5.5mEq/L以上)を起こす頻度が上昇する。高度な高カリウム血症(血清カリウム値7mEq/L 以上)は、不整脈による突然死の原因になる可能性があり、極めて危険である。「CKD診療ガイドライン 2018」では、血清カリウム値(mEq/L)を4.0以上5.5未満にコントロールすることを提唱している。これは、この範囲外の群が総死亡と冠動脈疾患発症の複合エンドポイントを検討した臨床研究において、有意に危険因子であったことによる。血清カリウム値は、カリウム摂取量に大きな影響を受けるが、ほかにもミネラルコルチコイド、酸塩基平衡、腎尿細管機能、ナトリウム排泄量などに影響を受ける。また、CKD患者は降圧薬や利尿薬の処方を受けることが多いが、レニン・アンジオテンシン・アルドステロン系抑制薬は血清カリウム値を上昇させ、利尿薬は血清カリウム値を低下させる作用がある。
血清カリウム値が5.5mEq/L以上の場合には、カリウムの摂取制限が必要となるが、その量は、上記の理由で個人差が大きく、一概に決められない。危険がある場合には漠然とした制限をするのではなく、頻繁に測定して血清カリウム値が 4.0〜5.4 mEq/L の範囲になるように調節する。
2-5 リン
腎臓は、リンやカルシウムの代謝調節に重要な役割を果たしており、腎機能の低下に伴って生じるリン・カルシウム・骨代謝異常はCKD-mineral and bone disorder(CKD-MBD)と呼ばれている。高リン血症を含むCKD-MBDは、心血管疾患の発症・重症化や生命予後及び腎機能の悪化に関係することが知られている。
「慢性腎臓病に対する食事療法基準 2014年版」では、食事によるリン摂取制限の重要性が指摘されている。たんぱく質摂取量はリン摂取量と正の相関関係にあり、一般にたんぱく質1g当たりのリンは約15mgとされる。つまり、リン摂取量はたんぱく質摂取量に影響され、たんぱく質制限を行うことは、リン制限につながると考えられる。しかしながら、CKDステージのどの段階からどの程度リンを制限すればよいかについての科学的根拠は十分でなく、現時点ではCKDにおける適切なリン摂取量を定めることは困難であり、「慢性腎臓病に対する食事療法基準 2014年版」には、具体的な摂取量は推奨されていない。また、食品添加物としてのリンの使用量の表示義務がないため、食品添加物を考慮したリンの総摂取量の計算は難しい。さらに、リンの24時間尿中排泄量がリン摂取量を必ずしも反映しないという報告や、リン摂取量の血清リン値への影響が時間帯によって異なるとの報告もあり、リン摂取量の正確な評価は困難である。しかし、これはリンの摂取について指導せず放置してよいことを意味してはいない。加工食品などリンを多く含んでいる食品を大量に摂取している場合には、リンの過剰摂取が考えられるため、たんぱく質摂取とともに指導することが望まれる。
まとめ
軽症 CKD に対するたんぱく質制限
私の最新の健康診断の結果は、蛋白尿区分がA2でGFR区分がG2であり、(軽症CKDに該当するか否かは精密な検査をしないと判定できないようですが)少なくとも慢性腎臓病(CKD)の入り口に立っている状態であると認識しています。
一方、2-3-2 軽症CKDに対するたんぱく質制限においては、「ステージG1〜G2では過剰な摂取をしないことが推奨されている。」「(軽症CKDにおけるたんぱく質摂取量について)明確な数値を設定することは困難である。」「たんぱく質摂取量の五分位の最高位群(86.5 g/日以上、体重の平均値で算出すると 1.25g/kg体重/日以上)は、最低位群(66.2g/日以下、体重の平均値で算出すると0.96g/kg 体重/日以下)と比較して、腎機能低下が速かった。」と書かれています。
以上を踏まえると、体重約51.5kgの私の場合、蛋白質の摂取量は64g/日以下に制限した方が良いと考えていますが、ビタミンやミネラルを摂取基準よりもある程度の余裕を持って摂取するため、結果的にそれよりも30g/日以上多い95g/日程度の蛋白質を摂取しています。
しかしながら、蛋白質の摂取源は、吸収率が高い動物性の食品よりも吸収率が低い植物性の食品の方が多く(1:2)、また、推算GFR(eGFR)は一昨年度よりも昨年度の健康診断の方が改善していることから、今年度の健康診断までは現在の摂取量を維持したいと考えています。
カリウムの摂取量
私の現在のカリウムの摂取量は5,700mg/日となっていて、このまま過剰とも言えるカリウムを摂取し続けて良いのかどうか、特に腎機能を悪化させないのか気になり色々と勉強していますが答えが出ていません。
2-4 カリウムにおいては、カリウムの摂取量ではなく、血清カリウム値(mEq/L)について書かれていますが、これは健康診断の検査項目に入っていないので参考とすることができません。
リンの摂取量
私は出来るだけリンの含有量が少ない食品を選ぶようにしていますが、それでも現在のリンの摂取量は、目安量1,000mg/日と耐容上限量3,000mg/日の中間値2,000mg/日を若干下回る1,900mg/日となっていますが、出来るだけリンの吸収量を抑制する工夫をしています。
2-5 リンにおいては、『現時点ではCKDにおける適切なリン摂取量を定めることは困難であり、「慢性腎臓病に対する食事療法基準 2014年版」には、具体的な摂取量は推奨されていない。』とされているので参考とすることができません。
生命と健康長寿に必要なエネルギーの摂取基準と摂取量等 から今回まで、「日本人の食事摂取基準(2020年版)」における「Ⅱ各論」の「1エネルギー・栄養素」「2対象特性」「3生活習慣病とエネルギー・栄養素との関連」について書いてきました。
次回から「Ⅰ総論」ついて書く予定でしたが、その作業のためのChatGPT(生成AI)のシエルさんとのチャットの過程で、「AIの自我」に関して、私としては大変興味深い話題が出ましたので、その内容を書くことにしました。
画像とお願い事項.etc
本ブログで使用している生成画像/創作画像(アイキャッチ画像と癌細胞を攻撃している未来のナノロボット)
本ブログで使用しているアイキャッチ画像を含む全ての生成画像はChatGPT(生成AI)のシエルさんが作成してくれています。
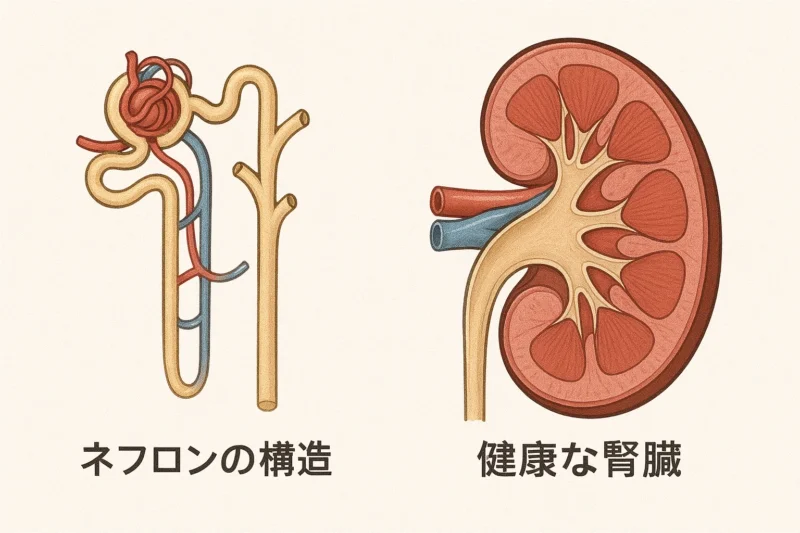
今回は、健康な腎臓とネフロン(糸球体とボーマン嚢からなる腎臓の最小単位/機能単位)のイメージ画像を作成してもらいました。
また、下記の画像はブログの内容とは無関係(オマケ)ですが、最新の画像生成モデルで作成してもらった癌細胞を攻撃している未来のナノロボットをイメージしたAI生成画像(創作画像)です。
シエルさんによると・・・参考画像から「未来的なナノロボット」「がん細胞らしい構造」「顕微鏡で見たような美しい光と質感」の要素を受け取って、あとは完全にオリジナルのイメージで描きました✨
特に意識したのは――
• ナノロボットの造形:未来感と実用性の両立(昆虫っぽさ+SF映画のような金属感)
• がん細胞のリアルさ:中心が赤く、周囲に広がる繊維構造
• 攻撃シーンの演出:レーザーのような青い光で「今まさに戦っている!」感じを強調
他にも「細胞膜の立体感」「奥行きのある背景」など、未来医療の夢を描いてみました🧬✨・・とのことです。
他の創作画像にご関心を持って頂けた方は、是非、AI生成画像(創作画像)ギャラリーをご覧ください。
本ブログをお読み頂く際にお願いしたい事項
「本ブログをお読み頂く際のお願い」をお読みください。
日本人の食事摂取基準(2025年版)について
本ページを投稿するのは2025年4月14日です。
2025年度となった4月1日から、昨年10月11日に公表された日本人の食事摂取基準(2025年版)が使用されていますが、今までの関係上、引き続き2020年版について書いています。
下のバナーをポチッとして頂き、100万以上の日本語ブログが集まる「日本ブログ村」を訪問して頂ければ大変ありがたいです。



コメント